2015年芝中学の問題です。
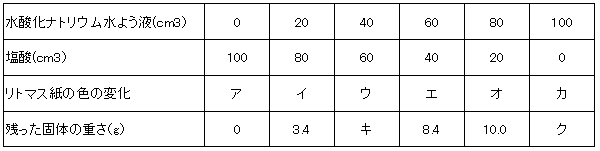
こさのちがう塩酸A、Bとうすい水酸化ナトリウム水よう液Cを使って次の実験を行いました。
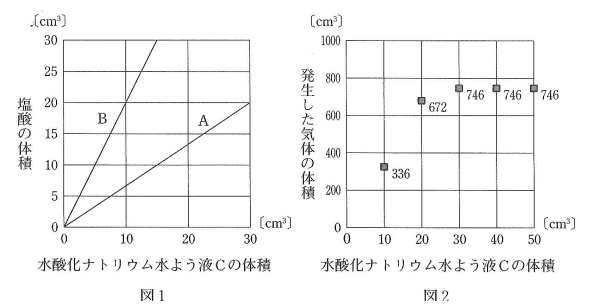
【実験1】 CにA、Bをそれぞれ加え、ちょうど中和させたときの体積の関係を調べると、図1の結果が得られました。
【実験2】 30cm3のCを蒸発皿にとり、水を蒸発させて残った①固体の重さを上皿てんびんではかると1.2gでした。また、20cm3のAと30cm3のCを混ぜ合わせ、水を蒸発させると1.8gの固体が残りました。
【実験3】 5本の試験管にアルミニウムを0.6gずつとり、それぞれにCを10cm3、20cm3、30cm3、40cm3、50cm3加え、十分に反応させました。このとき発生する気体の体積をはかった結果を図2のグラフに■で表しました。■の右の数値は発生した気体の体積〔cm3〕の値です。
【実験1】について
(1)2個のビーカーにCを20cm3ずつとり、一方のビーカーにAを15cm3加え、もう一方のビーカーにBを15cm3加えました。これらのビーカーにBTB液を少し加えると、それぞれ何色になりますか。
【実験2】について
(2)20cm3のAと20cm3のCを混ぜ合わせ、水を蒸発させると何gの固体が残りますか。 答が割り切れないときは、四捨五入して小数第1位まで求めること。
(3)10cm3のAと30cm3のCを混ぜ合わせ、水を蒸発させると何gの固体が残りますか。 答が割り切れないときは、四捨五入して小数第1位まで求めること。
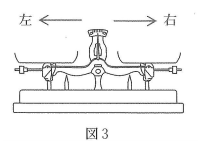
(4)下線部①について。上皿てんびんの使い方として正しい記述を次の中から1つ選んで、記号で答えなさい。ただし、記述内の左右は、てんびんを正面から見たときのものとします。(図3)
(ア)分銅は上部のつまみを人差し指と中指と親指でしっかりともつ。
(イ)右ききの場合、左の皿に薬包紙と固体をのせ、右の皿に薬包紙と分銅をのせる。
(ウ)右ききの場合、右のさらに薬包紙と固体をのせ、左の皿に分銅をのせる。左の皿には薬包紙をのせない。
(エ)重さをはかるときは、分銅を軽いものからのせ、少しずつ重いものに変えてつり合わせる。
(オ)重さのつり合いをしらべるためには、てんびんの針が完全に静止するまで待たなければならない。
【実験3】について
(5)発生した気体は何ですか。
(6)アルミニウム0.6gをすべてとかすのに必要なCは何cm3ですか。答が割り切れないときは、四捨五入して小数第1位まで求めること。
(7)Cを2倍にうすめた水よう液をりとします。Cの替わりにDを用いて同様に実験を行った場合、グラフはどのようになりますか。次の記述のうち、正しいものをすべて選んで、記号で答えなさい。
(ア)Dの体積が10cm3のとき、発生した気体の体積は336cm3と等しい
(イ)Dの体積が20cm3のとき、発生した気体の体積は672cm3よりも大きい
(ウ)Dの体積が30cm3のとき、発生した気体の体積は746cm3よりも大きい
(エ)Dの体積が40cm3のとき、発生した気体の体積は746cm3と等しい
(オ)Dの体積が40cm3のとき、発生した気体の体積は746cm3よりも小さい
(カ)Dの体積が50cm3のとき、発生した気体の体積は746cm3と等しい
(キ)Dの体積が50cm3のとき、発生した気体の体積は746cm3よりも小さい
(8)アルミニウムと同様に、Cにとけて気体を発生する物質を次の中から1つ選んで、記号で答えなさい。
(ア)鉄 (イ)マグネシウム (ウ)あえん (エ)石灰石 (オ)鋼
【解説と解答】
【実験1】グラフからB:C=2:1、A:C=2:3で中和することがわかります。
(1)A15cm3とC20cm3の場合、A15cm3とちょうど中和するCは22.5cm3になるので、まだ中和していないから酸性になります。したがってBTBは黄色に反応します。
一方Bが15cm3の場合はCが7.5cm3で中和しますが、Cは20cm3入っているので、アルカリ性になり、BTBは青色に反応します。
(答え)Aを入れたもの 黄色 Bを入れたもの 青色
【実験2】からCには30cm3に1.2gの水酸化ナトリウムが含まれ、それに20cm3の塩酸Aを加えると1.8gの食塩ができます。
(2)20cm3のAと20cm3のCでは中和はC20cm3分でするので、重さは1.8÷3×2=1.2gになります。
(答え)1.2g
(3)10cm3のAと30cm3のCだと中和はAによって決まり、Cが15cm3の中和ですから、食塩は0.9g。と残り15cm3の水酸化ナトリウムが残るのでその重さが1.2÷2=0.6gですから。、合計1.5gになります。
(答え)1.5g
(4)正しいものですから、イになります。分銅は手でもってはいけません。イが正しく右側に分銅をのせかえて調整するので、ウは誤り。エ、オも違います。
(答え)イ
【実験3】
(5)アルミニウムと塩酸ですから、発生する気体は水素です。
(答え)水素
(6)746÷672≒1.11ですから、20×1.11=22.2cm3
(答え)22.2cm3
(7)DはCを2倍に薄めたので、Cを半分いれるのと同じことになります。
Dが10cm3であればCを5cm3入れるのと同じになりますから、オとカが正しくなります。
(答え)オ、カ
(8)水酸化ナトリウムに反応するのは亜鉛です。
(答え)ウ
==============================================================
中学受験で子どもと普通に幸せになる方法、本日の記事は
はじめのうちは結果を問わない方が良い
==============================================================
今日の慶應義塾進学情報
社会常識
==============================================================

==============================================================
==============================================================

==============================================================
![]()
にほんブログ村