2015年桜蔭中学の問題です。
ある濃度の水酸化ナトリウム水よう液と塩酸がある。これらの水よう液をいろいろな量で混ぜた。その水よう液を、赤色と音色のリトマス紙にそれぞれ一滴ずつたらして色の変化を見たのち、しっかりと水分を蒸発させ、残った固体の重さを調べた。下の表は、混ぜ合わせた水よう液の体積と、実験の結果を表したものである。以下の問いに答えなさい。
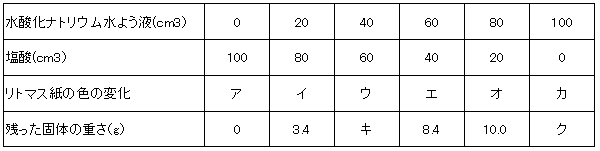
問1 リトマス紙の色の変化が以下の(a)~(c)の結果となるものは、表のア~カのどれですか。それぞれにあてはまるものをすべて選び、記号で答えなさい。あてはまるものがないときはXを書きなさい。
(a)赤色のリトマス紙が青く変化した
(b)赤色のリトマス紙も青色のリトマス紙もどちらも変化しなかった
(c)青色リトマス紙が赤く変化した
問2 表のキ、クにあてはまる数字を答えなさい。
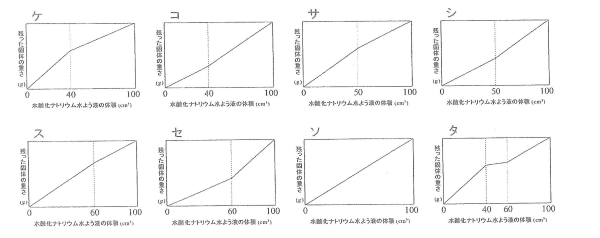
問3 混ぜた水酸化ナトリウム水よう液の体積と残った固体の重さの関係をグラフにすると、その形はどのようになりますか。ケ~タから選び、記号で答えなさい。
問1
(水酸化ナトリウム、塩酸)=(20、80)で中和していたとすると、(60、40)、(80、20)は水酸化ナトリウムだけが増えると考えられます。(20、80)から(60、40)は40cm3増えて5g固体が増えますが、(60、40)から(80、20)は20cm2で1.6gしか増えないので合いません。そこで
(水酸化ナトリウム、塩酸)=(40、60)で中和していたとすると、キ=6.8gとなり、(40、60)から(60、40)も、(60、40)から(80、20)も1.6g増えているので、これが正しいことになります。
もし(水酸化ナトリウム、塩酸)=(60、40)で中和していたとするとエは3.4×3=10.2gにならなければならないので、これも違います。
したがって
ア、イが酸性、ウが中性、エ、オ、カがアルカリ性になるので、(a)がエ、オ、カ。(b)がウ。(c)がア、イになります。
問2
したがってキ=6.8 クは10.0+1.6=11.6です。
(答え)キ 6.8 ク 11.6
問3
水酸化ナトリウムが40cm3で中和ですからグラフはケです。
==========================================================
中学受験で子どもと普通に幸せになる方法、本日の記事は
補欠は悩む
==============================================================
中学受験 算数オンライン塾
2月7日の問題
==============================================================

==============================================================
==============================================================

==============================================================
![]()
にほんブログ村


