2016年東邦大東邦中学の問題です。
次の文章を読み、あとの(1)~(6)の問いに答えなさい。ただし、BTB溶液は中性で緑色を示し、その体積は無視できるものとします。水酸化ナトリウムを溶かす前の水の体積と、溶かした後の水溶液の体積は等しいものとします。また、反応容器の内と外で熱のやりとりはないものとします。
水酸化ナトリウムは白色の固体で、水に溶けるときに熱が発生します。下の表は、20℃の水に溶かした水酸化ナトリウムの重さ、そのときの水の体積、できた水溶液の温度を表したものです。
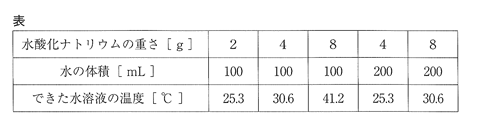
また、水酸化ナトリウム水溶液に塩酸を加えると、水溶液中に食塩ができ、この変化でも熱が発生します。
4gの水酸化ナトリウムを20℃の水100mLに溶かして作った水酸化ナトリウム水溶液にBTB溶液を加え、温度を20℃まで下げました。これに、ある濃さの20℃の塩酸Aを100mL加えると、溶液の色が緑色になりました。このときできた食塩水の温度は26.7℃でした。
次に、2gの水酸化ナトリウムを20℃の水50mLに溶かして作った水酸化ナトリウム水溶液にBTB溶液を加え、温度を20℃まで下げました。これに、20℃の塩酸Aを50mL加えると、溶液の色が緑色になりました。このときできた食塩水の温度は26.7℃ でした。
(1)4gの水酸化ナトリウムを20℃の水50mLに溶かしました。このときできた水溶液の温度は何℃ですか。
(2)(1)でできた水酸化ナトリウム水溶液にBTB溶液を加えました。これに塩酸Aを溶液の色が緑色になるまで加えました。このとき加えた塩酸Aの体積は何mLですか。
(3)6gの水酸化ナトリウムを水100mLに溶かしました。この水溶液にBTB溶液を加え、さらに塩酸Bを50mL加えたところ、溶液の色が緑色になりました。塩酸Bの濃さは塩酸Aの濃さの何倍ですか。
(4)(3)でできた食塩水の温度は何℃ですか。ただし、混合前の塩酸、水酸化ナトリウム水溶液の温度はともに20℃であるものとします。
(5)塩酸A50mLにBTB溶液を加えました。これに固体の水酸化ナトリウムを溶液の色が緑色になるまで加えました。このとき加えた水酸化ナトリウムの重さは何gですか。
(6)(5)でできた食塩水の温度は何℃ですか。ただし、水酸化ナトリウムを加える前の塩酸の温度は20℃であり、同じ量の水酸化ナトリウムを、水に溶かしたことによって発生する熱の量と、塩酸に溶かしたことのみによって発生する熟の量は等しいものとします。
【解説と解答】
(1)最初の水の温度は20℃でした。
4gの水酸化ナトリウムを入れたとき、30.6℃になっているので、10.6℃温度が上がっているから、10.6×100=1060 calの熱量が発生したことになります。
一方同じ4gの食塩を200mLの水に入れたときは25.3℃になって5.3℃温度が上がっているが、水が200mLなので5.3×200=1060calとなり、発生した熱量は変わっていないということになります。
したがって、50mLのときも1060cal発生しているから、1060÷50=21.2℃上がるから、20+21.2=41.2℃になります。
(答え)41.2℃
(2)
4gの水酸化ナトリウムを100mLの水に溶かしたとき、塩酸Aを100mL入れると中和しています。
2gの水酸化ナトリウムを50mLの水に溶かしたとき、塩酸Aを50mL入れると中和しています。
この2つの水酸化ナトリウム水溶液の濃さは同じですから、塩酸Aと1:1の比で中和しています。
(1)で作った水酸化ナトリウム水溶液は上の2倍の濃さになっているので、塩酸Aも2倍必要になるから50mL×2=100mLになります。
(答え)100mL
(3)
6gの水酸化ナトリウムを100mlの水に溶かした水溶液は4gの水酸化ナトリウムを水100mLに溶かしたものの1.5倍の濃さになります。
塩酸Bは50mLで中和したので、塩酸Aの1.5×2=3倍の濃さになります。
(答え)3倍
(4)
4gの水酸化ナトリウムを100mLの水に溶かした水溶液と塩酸Aを100mlまぜると、26,7℃になるので、6,7×200=1340calの熱量を発生しています。
2gの水酸化ナトリウムを50mLの水に溶かした水溶液と塩酸Aを50mlまぜると、同じく26,7℃になるので、6.7×100=670calの熱量を発生しています。
6gの水酸化ナトリウムが中和したとき、670×3=2010calの熱量を発生しています。で、このとき、全体の体積は150mLになっているので、2010÷150=13.4℃上がるから、20+13.4=33.4℃
(答え)33.4℃
(5)
塩酸A 50mLは2gの水酸化ナトリウムを50mLの水に溶かした水溶液と中和しています。
(答え)2g
(6)
このとき、まず水酸化ナトリウムが溶けることで発生する熱量は5.3×100=530cal発生します。
さらに中和で発生する熱量は670calですが、合計1200cal。容積は50mLですから、1200÷50=24℃上昇します。 20+24=44℃
(答え)44℃
「映像教材、これでわかる水溶液」(田中貴)
============================================================
受験で子どもと普通に幸せになる方法、本日の記事は
きれいに解くことにこだわらない
==============================================================
今日の慶應義塾進学情報
普通部の理科
==============================================================

==============================================================

==============================================================

==============================================================
![]()
にほんブログ村


